Mikrobiom jelitowy pacjentów z łuszczycą: Wpływ na patogenezę i potencjał terapeutyczny

Łuszczyca stanowi dość powszechną i przewlekłą chorobę zapalną skóry oraz stawów, która dotyczy około 2-4% ogólnej populacji (1). Przez wiele lat błędnie kojarzona jedynie z nadmierną proliferacją keratynocytów oraz charakterystyczną łuską na zmienionej chorobowo skórze. Obecnie za jej istotę uważa się zaburzenie układu odpornościowego (2), na który wpływ ma m.in. mikroflora jelitowa.
Według danych literaturowych łuszczyca wiąże się z częstszym współwystępowaniem innych chorób tj. choroby układu krążenia, nadciśnienie tętnicze, otyłość, zespół metaboliczny i nieswoiste zapalenie jelit (IBD)(3).
Łuszczyca stanowi dość powszechną i przewlekłą chorobę zapalną skóry oraz stawów, która dotyczy około 2-4% ogólnej populacji (1). Przez wiele lat błędnie kojarzona jedynie z nadmierną proliferacją keratynocytów oraz charakterystyczną łuską na zmienionej chorobowo skórze. Obecnie za jej istotę uważa się zaburzenie układu odpornościowego (2), na który wpływ ma m.in. mikroflora jelitowa.
Według danych literaturowych łuszczyca wiąże się z częstszym współwystępowaniem innych chorób tj. choroby układu krążenia, nadciśnienie tętnicze, otyłość, zespół metaboliczny i nieswoiste zapalenie jelit (IBD)(3).

Łuszczyca: Choroba o podłożu zapalnym i autoimmunologicznym
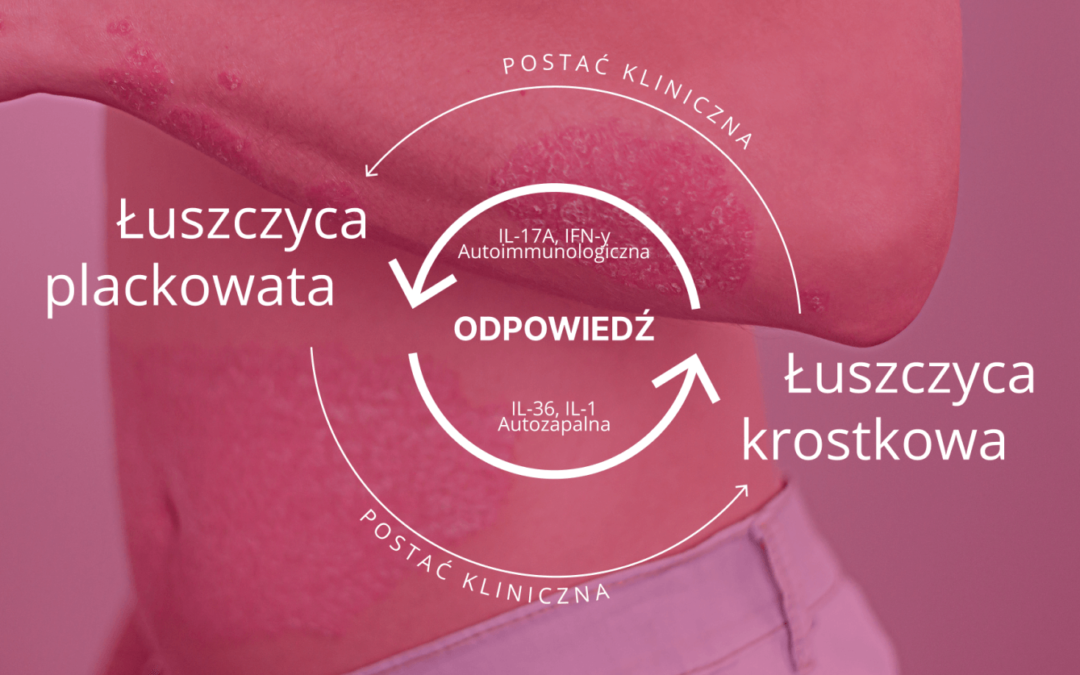
W patogenezie łuszczycy znajdziemy 2 rodzaje nieprawidłowych odpowiedzi immunologicznych: autoimmunologiczne i autozapalne. Zależności między nimi decydują o wystąpieniu określonej postaci choroby. Przykładem jest:
- łuszczyca plackowata z przewagą odpowiedzi autoimmunologicznej,
- łuszczyca krostkowa z dominacją odpowiedzi autozapalnej immunologicznej.

Dostępne dowody wskazują, że istnieją również inne podtypy kliniczne łuszczycy w spektrum między tymi dwoma fenotypami klinicznymi (4).
Mieszana odpowiedź autoimmunologiczna i autozapalna w łuszczycy
Choroby zapalne i autoimmunologiczne różnią się od siebie klinicznie. Reakcje autoimmunologiczne wiążą się z aktywacją nabytego układu odpornościowego np. komórek T lub B, podczas gdy reakcje autozapalne są napędzane przez endogenne sygnały zagrożenia, mediatory metaboliczne i/lub cytokiny. Jednakże w przypadku chorób tj. łuszczyca, te dwa procesy często ze sobą współistnieją i mogą oddziaływać na siebie. Stany zapalne mogą stanowić zmienną mieszaninę odpowiedzi autoimmunologicznych i autozapalnych (4).
Limfocyty immunosupresyjne w łuszczycy – rola Treg
Przeciwstawnie do opisanych procesów działają regulatorowe limfocyty T (Treg), które pełnią funkcję immunosupresyjną. Hamują nadmierne reakcje immunologiczne na różnorodne antygeny: antygeny własne, antygeny pochodzące od bakterii komensalnych oraz alergeny środowiskowe. W przypadku wielu chorób autoimmunologicznych i zapalnych tj. układowy rumień rumieniowy, choroby zapalne jelit, reumatoidalne zapalenie stawów oraz łuszczyca, obserwuje się charakterystyczne zmniejszenie zarówno liczby, jak i aktywności limfocytów Treg. Kluczową rolę w rozwoju, utrzymaniu i funkcjonowaniu limfocytów Treg odgrywa czynnik transkrypcyjny o nazwie Foxp3 (Forkhead box P3).
Na ekspresję tego czynnika wpływa wiele różnych czynników:

Mikrobiom jelitowy i łuszczyca: kluczowe zależności
Mikrobiota jelitowa ma ogromny wpływ na właściwe funkcjonowanie układu immunologicznego, w tym na różnicowanie limfocytów T i właściwą odpowiedź na bodźce immunologiczne. Nie bez powodu, budzi coraz większe zainteresowanie w chorobach z autoagresji tj. łuszczyca.
Zaburzona bariera jelitowa i translokacja bakteryjna
Za fundament zdrowia jelit uznaje się szczelną barierę jelitową. Naruszenie jej powoduje ogólnoustrojową dystrybucję bakterii lub ich metabolitów. Wpływa to na pracę układu odpornościowego i zaburza funkcjonowanie całego organizmu (6). Okazuje się, że problem przesiąkliwości bariery jelitowej może dotyczyć również pacjentów w łuszczycą. W jednym z badań w 2014 roku we krwi chorych z aktywną chorobą wykryto bakteryjne DNA i wyższy poziom cytokin zapalnych w surowicy. Przebieg choroby charakteryzował się również dłuższym czasem trwania i wcześniejszym początkiem w porównaniu do chorych bez tego rodzaju translokacji (7).
Dysbioza w łuszczycy
Badacze obserwują wiele zaburzeń mikrobiomu u osób cierpiących na łuszczycę. Stwierdza się istotny związek między zwiększoną kolonizacją skóry i jelit przez Staphylococcus aureus, Candida albicans i Malassezia a nasileniem objawów łuszczycy (12). Zespół badawczy pod kierunkiem dr Hidalgo-Cantabra zanotował w przypadku pacjentów z łuszczycą obniżenie populacji bakterii Bacteroides i Proteobacteria oraz wzrost Actinobacteria i Firmicutes w kale. Ponadto stosunek bakterii Firmicutes do Bacteroidetes u pacjentów z łuszczycą był zaburzony w porównaniu z grupą kontrolną zdrowych osób.
Bacteroides to bardzo ważna grupa bakterii odpowiedzialna za wytwarzanie krótkołańcuchowych kwasów tłuszczowych (SCFA), które biorą udział w stabilizacji ekspresji Foxp3 (odpowiadających funkcje limfocytów Treg)(9).
Mikrobiom jelitowy w IBD i łuszczycy – wspólne cechy
Zauważa się, że zmiany w mikrobiomie jelitowym u pacjentów z łuszczycą są zbliżone do tych obserwowanych u pacjentów z chorobami zapalnymi jelit. W przypadku obu chorób obserwuje się (10):
– obniżone poziomy: F.prausnitzii , Bifidobacterium spp., Lactobacillus spp., Parabacteroides i Coprobacillus
– podwyższoną liczebność: Salmonella spp., Campylobacter spp., Helicobacter spp., Escherichia coli, Alcaligenes spp. i Mycobacterium spp. (11).
Rola Faecalibacterium prausnitzii
F. prausnitzii to kluczowa bakteria świadcząca o zdrowiu jelit. Jest jednym z głównych producentów maślanu – krótkołańcuchowego kwasu tłuszczowego, który pełni wiele funkcji w organizmie m.in.:
- jest źródłem energii dla kolonocytów,
- odgrywa rolę w zmniejszaniu stresu oksydacyjnego,
- ma właściwości przeciwzapalne,
- bierze udział modulowaniu równowagi pomiędzy komórkami efektorowymi T a Treg.
Spadek liczebności bakterii komensalnej F. prausnitzii może wywierać skutki ogólnoustrojowe i wpływać nie tylko na jelita, ale także na skórę.
F.prausnitzii i E. coli w łuszczycy i współistniejącym IBD i samej łuszczycy
W badaniu z 2016 r. oceniono liczebność F. prausnitzii i E. coli u pacjentów z łuszczycą i chorobami zapalnymi jelit. Po wykonaniu analizy mikrobiomu porównano liczebność F. prausnitzii i E. coli w próbkach kału od zdrowych osób z grupy kontrolnej z próbkami pacjentów chorych na łuszczycę, IBD, a także w grupie chorującej na obie te choroby. U badanych z łuszczycą w kale występowała istotnie mniejsza ilość F. prausnitzii w porównaniu do zdrowych osób z grupy kontrolnej. Podobne wartości obserwowano u pacjentów z IBD. Wraz ze zmniejszonym poziomem F. prausnitzii u pacjentów z łuszczycą występowała istotnie większa liczebność E. coli (13). W łuszczycy zaobserwowano występowanie łagodnego zapalenie jelit, co pozwala na hipotezę, że mikroflora jelitowa może być zaangażowana w łuszczycę(14).
Wpływ grzybów Candida na łuszczyce
Poza bakteriami w skład mikrobiomu jelitowego wchodzą również grzyby. Gatunki Candida są częścią fizjologicznej mikrobioty człowieka i kolonizują błony śluzowe przewodu pokarmowego. Gdy dojdzie to ich przerostu, mogą spowodować oportunistyczną infekcję (15). Na podstawie metanaliz stwierdzono, że częstość występowania Candida spp. jest istotnie wyższa u pacjentów z łuszczycą w porównaniu z grupą kontrolną (16). Wykazano, że antygeny (zwłaszcza białka powierzchniowe Candida albicans) mają działanie podobne do superantygenów powodujących aktywację limfocytów T i nadmierne uwalnianie cytokin prozapalnych (17). Mechanizmy zaangażowane w obronę gospodarza przed C. albicans mają natomiast podobne szlaki związane z patogenezą łuszczycy.
Zauważa się większe ryzyko przerostu Candidy w trakcie leczenia biologicznego łuszczycy. Konieczne są przyszłe badania w celu zbadania interakcji pomiędzy Candida spp., a układem odpornościowym w celu uzyskania potencjalnych, nowych opcji terapeutycznych ukierunkowanych na mikrobiom.
Potencjał terapeutyczny: Probiotyki, prebiotyki i przeszczep mikroflory jelitowej
Jak pokazują badania, różnorodność mikroflory jelitowej pacjentów chorych na łuszczycę jest znacznie zmniejszona. Wydaje się, że potencjalnym sposobem wspierania terapii może być modulacja flory jelitowej. Elementami tej strategii są probiotyki, prebiotyki i przeszczepianie bakterii kałowych (18).
Obecnie wciąż pojawiają się nowe badania przedkliniczne i badania kliniczne wykorzystujące probiotyki w leczeniu łuszczycy. Zauważa się ich potencjalne działanie:
- zmniejszenie zmian łuszczycowych i wskaźników ich nasilenia,
- hamowanie markerów zapalenia łuszczycy,
- regulacja komórek odpornościowych,
- modulowanie składu mikroflory (19).
W kale chorych na łuszczyce zauważa się niskie poziomy krótkołańcuchowych kwasów tłuszczowych (SCFA), które promują równowagę wśród komórek tj. Th1/Th2 i Th17/Treg. Warto zaznaczyć, że za produkcję SCFA odpowiadają bakterie jelitowe fermentujące prebiotyki (20). W ostatnich latach naukowcy obserwują niepokojący wzrost liczby chorych na łuszczycę w Japonii. Korelują to zjawisko ze zmianą nawyków żywieniowych na „zachodnie”, które zaburzają rdzenną mikroflorę jelitową. Wśród nowych nawyków żywieniowych obserwuje się zmniejszenie zawartości błonnika pokarmowego w diecie, co wpływa na spadek SCFA w mikroflorze jelitowej (5).
Probiotykoterapia w łuszczycy – badanie pilotażowe
W pilotażowym badaniu w 2020 roku na grupie pacjentów z łuszczycą i łuszczycowym zapaleniem stawów oceniono skuteczność wieloszczepowej mieszanki probiotycznej zawierającej 9 szczepów bakteryjnych: Lactobacillus casei W56, Lactobacillus acidophilus W22, Lactobacillus paracasei W20, Bifidobacterium lactis W51, Lactobacillus salivarius W24, Lactococcus lactis W19, Bifidobacterium lactis W52, Lactobacillus plantarum W62, Bifidobacterium bifidum W23 .
Po 12 tygodniach stosowania preparatu zaważono statystycznie istotną redukcję markerów stanu zapalnego i przepuszczalności jelit oraz poprawę jakości życia pacjentów. Pokazuje to potencjał tego rodzaju interwencji w grupie chorych na łuszczycę (21).
Perspektywy przyszłych badań — oś jelitowo-skórna
Najnowsze badania nad mikroflorą jelitową oraz mechanizmami regulacji układu odpornościowego sugerują, że różnego rodzaju zaburzenia wśród drobnoustrojów jelitowych oddziałują na procesy immunologiczne. Dzieje się tak m.in. poprzez zakłócanie funkcji limfocytów Treg oraz aktywację limfocytów Th17, co może przyczyniać się np. do rozwoju łuszczycy u osób genetycznie predysponowanych.
Kierunek badawczy skupiający się na jelitowo-skórnej zapowiada się jako obiecujący obszar przyszłych badań. Może on dostarczyć istotnych informacji, które pozwolą opracować bardziej kompleksowe i przyczynowe metody leczenia schorzeń dermatologicznych, w tym łuszczycy.
Bibliografia:
- Boehncke W. H., Schön M. P. Psoriasis. 2015;386(9997):983–994. doi: 10.1016/S0140-6736(14)61909-7
- Eberle F. C., Brück J., Holstein J., Hirahara K., Ghoreschi K. Recent advances in understanding psoriasis. 2016;5 doi: 10.12688/f1000research.7927.1
- Scher JU, Ubeda C., Artacho A., Attur M., Isaac S., Reddy SM Zmniejszona różnorodność bakteryjna charakteryzuje zmienioną mikroflorę jelitową u pacjentów z łuszczycowym zapaleniem stawów, przypominającą dysbiozę w chorobie zapalnej jelit. Artretyzm. Reumatol. 2015; 67 :128–139. doi: 10.1002/art.38892.
- Eberle F. C., Brück J., Holstein J., Hirahara K., Ghoreschi K. Recent advances in understanding psoriasis. 2016;5 doi: 10.12688/f1000research.7927.1
- Yun Liang, Psoriasis: A mixed autoimmune and autoinflammatory disease, Curr Opin Immunol. 2017 Dec; 49: 1–8.
- Komine, Recent Advances in Psoriasis Research; the Clue to Mysterious Relation to Gut Microbiome, Int J Mol Sci. 2020 Apr; 21(7): 2582
- Martin A.M., Sun E.W., Rogers G.B., Keating D.J. The Influence of the Gut Microbiome on Host Metabolism Through the Regulation of Gut Hormone Release. Front. Physiol. 2019;10:428. doi: 10.3389/fphys.2019.00428
- Ramírez-Boscá A., Navarro-López V., Martínez-Andrés A., Such J., Francés R., Horga de la Parte J., Asín-Llorca M. Identification of Bacterial DNA in the Peripheral Blood of Patients With Active Psoriasis. Jama Derm. 2015;151:670–671. doi: 10.1001/jamadermatol.2014.5585
- Hidalgo-Cantabrana C., Gómez J., Delgado S., Requena-López S., Queiro-Silva R., Margolles A., Coto E., Sánchez B., Coto-Segura P. Gut microbiota dysbiosis in a cohort of patients with psoriasis. Br. J. Dermatol. 2019;181:1287–1295. doi: 10.1111/bjd.17931
- Smith P.M., Howitt M.R., Panikov N., Michaud M., Gallini C.A., Bohlooly-Y. M., Glickman J.N., Garrett W.S. The microbial metabolites, short-chain fatty acids, regulate colonic Treg cell homeostasis. Science. 2013;341:569–573. doi: 10.1126/science.124116
- Irmina Olejniczak-Staruch, Alterations of the Skin and Gut Microbiome in Psoriasis and Psoriatic Arthritis, Int J Mol Sci. 2021 Apr; 22(8): 3998.
- Alesa D.I., Alshamrani H.M., Alzahrani Y.A., Alamssi D.N., Alzahrani N.S., Almohammadi M.E. The role of gut microbiome in the pathogenesis of psoriasis and the therapeutic effects of probiotics. J. Family Med. Prim. Care. 2019;8:3496–3503
- Fry L., Baker B.S. Triggering psoriasis: The role of infections and medications. Clin. Dermatol. 2007;25:606–615. doi: 10.1016/j.clindermatol.2007.08.015
- Eppinga H., Sperna Weiland C.J., Thio H.B., van der Woude C.J., Nijsten T.E.C., Peppelenbosch M.P., Konstantinov S.R. Similar depletion of protective Faecalibacterium prausnitzii in psoriasis and inflammatory bowel disease, but not in hidradenitis suppurativa. J. Crohns Colitis. 2016;10:1067–1075. doi: 10.1093/ecco-jcc/jjw070
- Scarpa R Manguso F D’Arienzo A et al. Microscopic inflammatory changes in colon of patients with both active psoriasis and psoriatic arthritis without bowel symptoms . J Rheumatol 2000 ; 27 : 1241 – 6
- Kühbacher A., Burger-Kentischer A., Rupp S. Interaction of Candida species with the skin. 2017;5(2) doi: 10.3390/microorganisms5020032
- Aldona Pietrzak; Prevalence and Possible Role of Candida Species in Patients with Psoriasis: A Systematic Review and Meta-Analysis, Mediators Inflamm. 2018; 2018: 9602362
- Kashem S. W., Kaplan D. H. Skin immunity to Candida albicans. 2016;37(7):440–450. doi: 10.1016/j.it.2016.04.007
- Chen L., Li J., Zhu W., et al. Skin and gut microbiome in psoriasis: gaining insight into the pathophysiology of it and finding novel therapeutic strategies. Frontiers in Microbiology . 2020;11 doi: 10.3389/fmicb.2020.589726.
- Lu X. Y. The randomized, double blind and control study of Probiotics in the treatment of psoriasis vulgaris. China Modern Medicine . 2017;24
- Haidmayer A, et. al. Effects of Probiotic Strains on Disease Activity and Enteric Permeability in Psoriatic Arthritis-A Pilot Open-Label Study. Nutrients. 2020).
Pozostałe artykuły
ROLA JELIT W TERAPIACH TRYCHOLOGICZNYCH
Jak to możliwe, aby kosmki jelitowe będące częścią przewodu pokarmowego wpływały na mieszki włosowe lub na skórę? Pierwszą wskazówkę znajdujemy już na samym początku. Jest to moment po zapłodnieniu, gdy w kobiecym łonie kształtowany jest zarodek. Łączące i powielające się komórki podzielone są na 3 warstwy tzw. listki zarodkowe. Kluczowy dla tematu osi jelito-skóra jest listek zarodkowy o nazwie ektoderma. To zbiór komórek, z których powstają: jelita, układ nerwowy oraz skóra ze swoimi przydatkami.
MIKROBIOTA JELITOWA DZIECKA A KOLKA NIEMOWLĘCA
Kolka niemowlęca jest jednym z najczęstszych zaburzeń czynnościowych przewodu pokarmowego występujących u dzieci w pierwszych miesiącach życia. Zaburzenie to dotyka nawet 20 % niemowląt. Najczęściej pojawia się w okresie od 1 miesiąca do 3 miesiąca życia, choć nawet 10 % niemowląt będzie doświadczało nieprzyjemnych objawów kolki w kolejnych miesiącach życia.
OTYŁOŚĆ – WIELOCZYNNIKOWA CHOROBA O PODŁOŻU ZAPALNYM. ROLA MIKROBIOMU JELITOWEGO
Otyłość to wieloczynnikowa choroba o podłożu zapalnym. Wobec najnowszej wiedzy nie można jej uznawać za schorzenie, którego przyczyna tkwi tylko w nadmiernej podaży kalorii. Choroba ta jest spowodowana różnymi czynnikami: genetycznymi i poza-genetycznymi (środowiskowymi). Często współwystępuje z zaburzeniami metabolizmu lipidów i glukozy, przewlekłym stanem zapalnym, stresem oksydacyjnym i zwiększonym ryzykiem różnych chorób, w szczególności chorób układu krążenia, cukrzycy i nowotworów. Jednym z najciekawszych czynników badanych w patogenezie otyłości jest wpływ mikroflory jelitowej na pojawienie się i rozwój tej choroby.